La mort, quelles limites, quelles pratiques ?
Modifié le :

Article rédigé en juin 2023 par
VALÉRIE MILS, Maître de conférence en biologie cellulaire - centre de biologie du développement - Université Paul Sabatier à ToulouseA l’heure ou le muséum de Toulouse propose une exposition sur les corps préservés, les scientifiques s’interrogent encore sur la façon dont il faut définir la mort elle-même. La mort, c’est l’interruption de la vie et des fonctions biologiques qui la caractérise. C’est aussi la perte de la conscience, de la personnalité, de tout ce qui fait de nous un être sensible et social.
La vie et la mort, deux concepts qui ne s’excluent pas mutuellement !
La mort est un processus qui prend son temps puisque, excepté les cas de morts violentes ou accidentelles, elle est l’issue inévitable du vieillissement irréversible de nos organes. Ce vieillissement est dû à l’altération de nos cellules par des stress issus de notre environnement (UV, polluants,…) mais aussi des stress endogènes liés à notre métabolisme, tel que la production de radicaux libres. Les cellules dont le génome est trop altéré par ces agressions ont le pouvoir de s’autodétruire par un processus appelé apoptose.
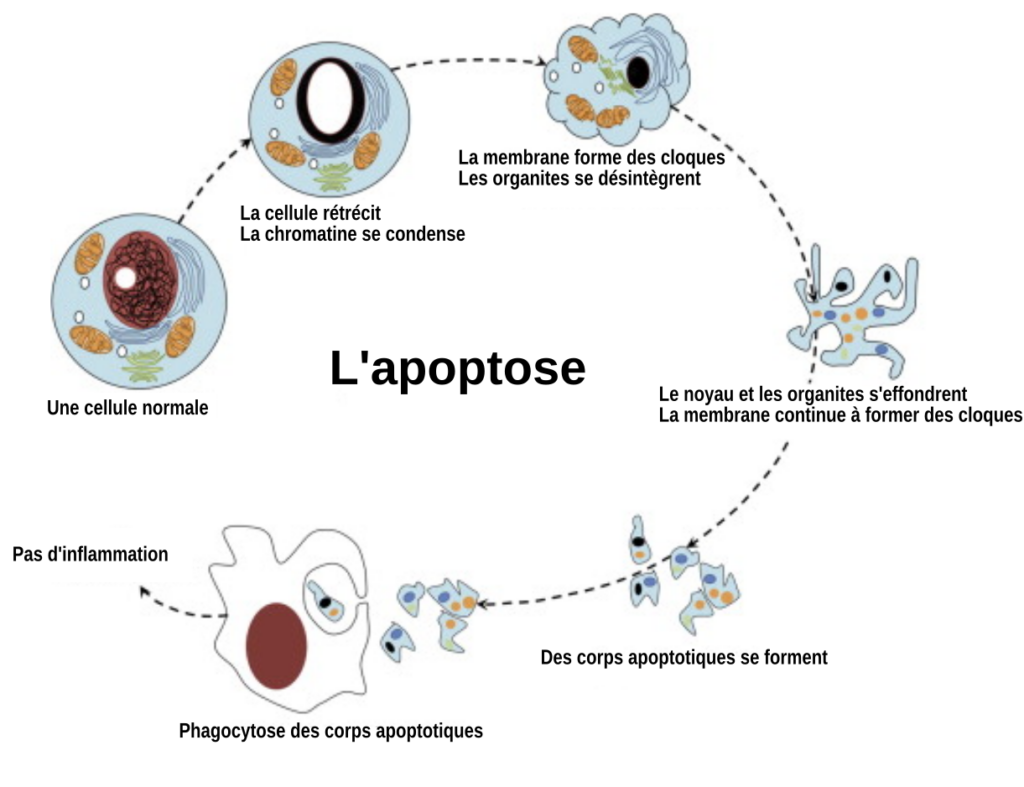
Ce phénomène suit un programme respectant des étapes précises et identiques quel que soit le type cellulaire. La cellule rétrécit suite à la condensation de son cytoplasme et de la chromatine nucléaire. Des vacuoles se forment où sont dégradés les organites comme les mitochondries et, dans le noyau, l’ADN est découpé par des nucléases en tronçons de plus en plus petits. Au terme de ce processus, la cellule se disloque en fragments de taille hétérogène appelés « corps apoptotiques » qui peuvent contenir des portions de noyau et qui sont empaquetés dans la membrane cellulaire. La présence de cette membrane évite que le cytoplasme et les produits de dégradation ne se répandent dans le milieu extracellulaire ce qui empêche le développement de réactions inflammatoires. Les corps apoptotiques sont finalement éliminés en étant phagocytés par les cellules situées à proximité . En soit, ce « suicide » cellulaire est une bonne chose car il évite l’accumulation de cellules anormales et dysfonctionnelles, sources potentielles de maladie. Chez les organismes jeunes et en bonne santé, les cellules ainsi éliminées sont remplacées par la production de nouvelles cellules à partir de réservoirs constitués de cellules souches adultes, présents dans la plupart des tissus. Ces cellules ont gardé des caractéristiques de cellules embryonnaires : elles ont un potentiel de division très élevé et produisent de nouvelles cellules capables d’acquérir les propriétés nécessaires au fonctionnement du tissu. Par exemple, dans l’intestin, les cellules de l’épithélium de surface qui subissent de gros stress mécaniques et chimiques sont éliminées au bout de 3 jours mais sont continuellement remplacées par l’activité de cellules souches situées à l’abri au fond des cryptes intestinales. L’apoptose est un processus qui peut même avoir lieu au cours du développement embryonnaire ou pendant l’enfance. Dans ce cas, elle est nécessaire au modelage des organes définitifs. La mort cellulaire peut donc être dissociée de la mort de l’individu.
En fait, le vieillissement n’est pas dû à l’élimination régulière des cellules abimées mais à la perte progressive de la capacité des cellules souches à les remplacer. Au cours du vieillissement, les cellules souches perdent leur capacité à se diviser. Le renouvellement des tissus se fait donc de moins en moins bien ce qui entraîne un fonctionnement moins efficace des organes et l’apparition de maladies. Le vieillissement des cellules souches est donc à l’origine du vieillissement de l’individu lié à la perte de fonction progressive des organes, ce qui le rapproche inéluctablement de la mort.
Toutefois, la mort de l’individu, même âgé, n’est pas la conséquence directe de la mort des organes et des cellules qui les composent. Dans un cadavre, de nombreuses cellules survivent pendant plusieurs heures voire plusieurs jours. Une personne venant de mourir conserve des organes constitués de cellules vivantes mais qui ont perdu la capacité d’assurer correctement leur fonction et de communiquer entre eux. Le corps juste décédé est comme un orchestre où chaque musicien joue sa partition sans chef d’orchestre. S’en suit une cacophonie qui ne ressemble plus en rien à la symphonie que les joueurs devraient produire.
Lequel du cœur ou du cerveau lâche le premier ?
La mort n’est donc pas instantanée. De plus, il semble qu’elle suive une chronologie déterminée. Dans le cas de mort naturelle, elle débute souvent par un arrêt cardio-respiratoire. L’arrêt de la respiration empêche l’oxygénation du sang et l’arrêt du cœur stoppe l’irrigation des organes par ce sang oxygéné. Or les neurones du cerveau sont extrêmement sensibles à la privation en oxygène. Pourtant, une activité cérébrale peut être maintenue pendant plusieurs minutes. Pour cette raison, depuis 1968, l’arrêt cardio-respiratoire n’est plus considéré comme suffisant pour déclarer l’individu mort et le critère de décès est aujourd’hui l’arrêt du fonctionnement du cerveau ou mort encéphalique. Mais là aussi, les choses sont moins simples qu’elles n’y paraissent car les neurones peuvent s’arrêter de fonctionner dans certaines zones du cerveau et pas d’autres. Par exemple, le tronc cérébral qui est le siège des fonctions vitales comme le contrôle de la pression sanguine et de la respiration peut fonctionner parfaitement alors que le cortex, siège de la conscience et de la pensée, peut être détruit. Et l’inverse est aussi vrai. Alors comment vérifier que le cerveau a intégralement cessé de fonctionner ? En France, on procède à une angiographie cérébrale, un examen radiologique permettant de vérifier que la circulation sanguine dans le cerveau s’est arrêtée. Un second critère possible est l’obtention de deux électroencéphalogrammes (EEG) plats pendant au moins 30min et effectués à 4h d’intervalle attestant que le cerveau du patient n’a plus d’activité électrique.
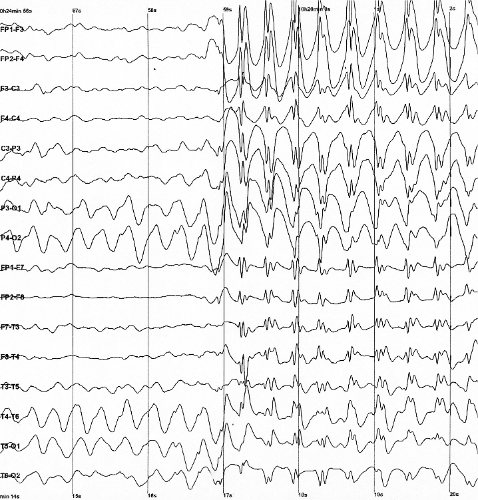
Il va sans dire que ces tests ne sont pas à la portée de tous les médecins qui doivent constater le décès de personnes hors milieu hospitalier. Ce type de contrôle est donc le plus souvent réservé aux sujets éligibles au don d’organes. Toutefois, vu le nombre croissant de patients en attente de greffe, la loi a récemment été modifiée : sont aussi considérées comme personnes décédées celles qui sont en arrêt cardio-respiratoire et qui ne montrent aucun signe de vie après 30min de soins intensifs en vue d’une réanimation. Les médecins considèrent qu’au bout de 30min, le cerveau privé d’irrigation sanguine est irrémédiablement détruit et donc que le patient est mort. On parle alors de «mort par arrêt cardio-respiratoire persistant ou réfractaire». Certains médecins doutent du bien fondé de telles pratiques car le constat de mort dépend directement de l’efficacité de la réanimation pratiquée et peut-être du savoir-faire des réanimateurs… De plus, certains contestent la recevabilité du critère arguant que certains patients en état d’hypothermie ou d’intoxication sévère aux benzodiazépines peuvent également produire des EEG plats.
Qu’advient-t-il du cerveau après l’arrêt cardiorespiratoire ?
Les études portant sur ce sujet sont bien sûr très rares chez l’humain. A ce jour, elles se résument à un travail mené sur 9 sujets humains souffrant d’atteintes cérébrales sévères et irréversibles. Le processus de mort encéphalique a été suivi sur ces sujets grâce à une électrocorticographie c’est-à-dire un enregistrement de l’activité électrique du cerveau en plaçant les électrodes directement à la surface du cortex cérébral ce qui permet de mesurer des activités électriques très faibles qui seraient indécelables par un EEG classique. La plupart des autres données publiées sont issues de travaux réalisés chez l’animal. L’ensemble des observations montre que la mort encéphalique ne résulte pas d’un arrêt progressif de l’activité des neurones mais fait suite au contraire à deux phases d’activité distinctes.

Tout d’abord, environ 20 secondes après l’arrêt cardio-respiratoire, on observe un pic d’ondes gamma, ondes qui sont habituellement associées aux états de concentration ou de remémoration. Après ce premier pic d’onde gamma, le cerveau se met en veille. Les neurones modifient leur métabolisme de façon à produire de l’énergie avec un apport limité en oxygène. Leur activité électrique se réduit drastiquement au point de générer un EEG plat. Pourtant le cerveau n’est pas encore mort. Entre cinq et dix minutes après l’arrêt cardio-respiratoire, les neurones les plus sensibles au manque d’oxygène commencent à se dépolariser c’est-à-dire que la différence de charge électrique entre l’intérieur et l’extérieur de la cellule s’annule. Les neurones relarguent alors des quantités massives de glutamate, un neuromédiateur excitateur essentiel du système nerveux central mais qui est neurotoxique à forte dose. Ce phénomène est d’abord localisé puis s’étend de proche en proche en quelques minutes à l’ensemble de l’encéphale à la vitesse de 50µ/sec. On ignore exactement où débute cette vague de dépolarisation mais on peut supposer qu’elle apparait dans les zones cérébrales dont la densité cellulaire est élevée et le besoin en oxygène important. C’est le cas de l’hippocampe et de la région tempo-pariétale. Curieusement, la stimulation de cette région provoque chez le sujet des sensations de décorporation similaires à ce que décrivent les sujets ayant fait l’expérience d’une mort imminente. Il se pourrait donc que les phénomènes dont témoignent ces sujets soient liés à la dépolarisation des neurones de cette région. Cette vague de dépolarisation appelée « vague de mort » est le dernier signe d’activité cérébrale que nos méthodes d’enregistrement actuelles peuvent mettre en évidence. Mais jusqu’à quel point le processus est-il irréversible ? Une équipe de chercheurs a testé les effets d’une reperfusion du cerveau en oxygène juste avant cette vague de mort et a obtenu une restauration de l’activité cérébrale dans 60% des cas ! Toutefois, il faut rester prudent avec cette méthode de réanimation par reperfusion en oxygène : fourni en excès, l’oxygène entraîne la formation de radicaux libres très toxiques pour les neurones. Le rétablissement brutal d’un flux sanguin oxygéné est d’ailleurs responsable de la plupart des décès de patients réanimés après arrêt cardio-respiratoire.
Au-delà de la mort encéphalique débutela mort progressive et désynchronisée des différents organes. Après les neurones, les premières cellules à mourir sont celles qui tapissent nos vaisseaux sanguins. Les vaisseaux se rompent, le sang s’échappe vers les tissus ce qui est à l’origine de l’apparition des lividités cadavériques. Le pancréas et le foie sont altérés par les enzymes digestives qu’ils fabriquent et suivent en moins de trente minutes. Les muscles qui contiennent de grandes réserves d’énergie tiennent un peu plus longtemps. Les cellules de la peau, des os et de la cornée sont celles qui résistent le plus longtemps, jusqu’à un jour ou deux. La décomposition des tissus commence 24h après le décès. Outre l’autolyse des cellules, la nécrose ou l’effet destructeur des enzymes digestives, les très nombreuses bactéries que nous transportons participent activement à la décomposition. En absence d’un système immunitaire efficace, les différents microbiotes avec lesquels nous vivons en symbiose durant notre vie (en particulier le microbiote intestinal) se transforment au moment du décès en prédateurs qui envahissent nos tissus, y prolifèrent et les digèrent.
Photo d’en tête : squelette penseur sur la notion de mort dans l’espace d’exposition « Momies, corps préservés, corps éternels (2023) » du Muséum de Toulouse. Crédit : Patrice Nin

